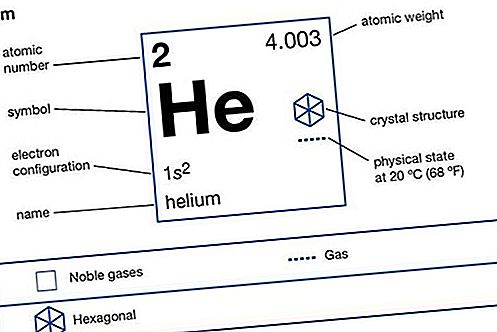
थोरियम (Th), आवधिक तालिका के एक्टिनोइड श्रृंखला के रेडियोधर्मी रासायनिक तत्व, परमाणु संख्या 90; यह एक उपयोगी परमाणु रिएक्टर ईंधन है। थोरियम की खोज (1828) स्वीडिश रसायनज्ञ जोन्स जैकब बर्जेलियस द्वारा की गई थी। यह सिल्वर व्हाइट है लेकिन हवा के संपर्क में आने पर ग्रे या काला हो जाता है। यह सीसे की तुलना में लगभग आधा है और पृथ्वी की पपड़ी में यूरेनियम की तुलना में तीन गुना अधिक प्रचुर मात्रा में है। थोरियम व्यावसायिक रूप से खनिज मोनाजाइट से पुनर्प्राप्त होता है और अन्य खनिजों जैसे कि थोराइट और थोरियानाइट में भी होता है। थोरियम धातु वाणिज्यिक मात्रा में tetrafluoride की (THF कमी से उत्पादन किया गया है 4) और (यद्यपि डाइऑक्साइड 2) और टेट्राक्लोराइड इलेक्ट्रोलिसिस (ThCl द्वारा 4)। तत्व का नाम नॉर्स भगवान थोर के लिए रखा गया था।
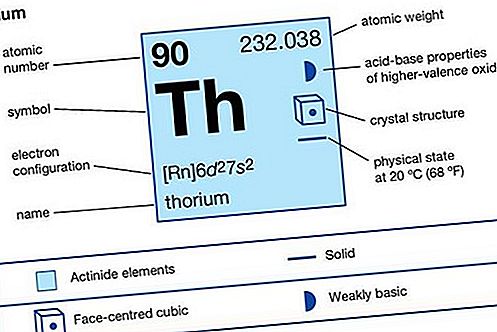

एक्टिनोइड तत्व: एक्टिनॉइड के व्यावहारिक अनुप्रयोग
थोरियम, भी, महान आर्थिक मूल्य के संभावित है, क्योंकि इसके आइसोटोप, थोरियम -232 में से एक में परिवर्तित किया जा सकता है
।
धातु को बाहर निकाला जा सकता है, लुढ़काया जा सकता है, जाली बनाया जा सकता है, झुलसा जा सकता है, और थूक दिया जा सकता है, लेकिन थोरियम की कम तन्यता के कारण ड्राइंग करना मुश्किल है। यह और अन्य भौतिक गुण जैसे कि पिघलने और क्वथनांक कुछ अशुद्धियों, जैसे कार्बन और थोरियम डाइऑक्साइड की छोटी मात्रा से बहुत प्रभावित होते हैं। थोरियम को मैग्नीशियम और मैग्नीशियम मिश्र धातुओं में जोड़ा जाता है ताकि उनकी उच्च तापमान शक्ति में सुधार हो सके। इसका उपयोग वाणिज्यिक फोटोइलेक्ट्रिक कोशिकाओं में तरंग दैर्ध्य के पराबैंगनी प्रकाश को मापने के लिए किया जाता है, जो 2000 से 3750 के एंगस्ट्रॉम तक होता है। ग्लास में जोड़ा गया, थोरियम एक उच्च अपवर्तक सूचकांक के साथ चश्मा देता है, विशेष ऑप्टिकल अनुप्रयोगों के लिए उपयोगी है। यह पहले गैस और केरोसीन लैंप के लिए एक घटक के रूप में बड़ी मांग में था और लाइटबल्ब्स और वैक्यूम ट्यूबों के लिए टंगस्टन फिलामेंट्स के निर्माण में इसका उपयोग किया गया है।
थोरियम की रेडियोधर्मिता स्वतंत्र रूप से (1898) जर्मन रसायनज्ञ गेरहार्ड कार्ल श्मिट और फ्रेंच भौतिक विज्ञानी मैरी क्यूरी द्वारा पाई गई थी। प्राकृतिक थोरियम रेडियोधर्मी समस्थानिकों का एक मिश्रण है, मुख्य रूप से बहुत लंबे समय तक रहने वाले थोरियम -232 (1.40 × 10 10 -आधे जीवन), थोरियम रेडियोधर्मी क्षय श्रृंखला के जनक। अन्य आइसोटोप यूरेनियम और एक्टिनियम क्षय श्रृंखला में स्वाभाविक रूप से होते हैं, और थोरियम सभी यूरेनियम अयस्कों में मौजूद होता है। थोरियम -232 ब्रीडर रिएक्टरों में उपयोगी है क्योंकि धीमी गति से चलने वाले न्यूट्रॉन को कैप्चर करने पर यह विखंडनीय यूरेनियम -233 में हो जाता है। सिंथेटिक आइसोटोप तैयार किए गए हैं; थोरियम -229 (7,880-वर्षीय अर्ध-जीवन), सिंथेटिक एक्टिनॉइड तत्व नेप्ट्यूनियम में उत्पन्न होने वाली क्षय श्रृंखला में बनता है, जो साधारण थोरियम (थोरियम -232) के लिए एक अनुरेखक के रूप में कार्य करता है।
थोरियम अपने लगभग सभी यौगिकों में +4 के ऑक्सीकरण राज्य को प्रदर्शित करता है। Th 4+ आयन कई जटिल आयन बनाता है। डाइऑक्साइड (ThO 2), एक बहुत ही दुर्दम्य पदार्थ है, जिसमें कई औद्योगिक अनुप्रयोग हैं; थोरियम नाइट्रेट एक वाणिज्यिक नमक के रूप में उपलब्ध रहा है।
तत्व गुण
| परमाणु क्रमांक | 90 |
|---|---|
| परमाण्विक भार | 232.038 |
| गलनांक | लगभग 1,700 ° C (3,100 ° F) |
| क्वथनांक | लगभग 4,000 ° C (7,200 ° F) |
| विशिष्ट गुरुत्व | लगभग 11.66 (17 ° C) |
| ऑक्सीकरण अवस्था | 4 |
| गैसीय परमाणु अवस्था का इलेक्ट्रॉन विन्यास | [आरएन] ६ डी २ 2 एस २ |