कार्बाइड, रासायनिक यौगिकों के किसी भी वर्ग जिसमें कार्बन को एक धातु या अर्धवृत्ताकार तत्व के साथ जोड़ा जाता है। कैल्शियम कार्बाइड मुख्य रूप से एसिटिलीन और अन्य रसायनों के स्रोत के रूप में महत्वपूर्ण है, जबकि सिलिकॉन, टंगस्टन, और कई अन्य तत्वों के कार्बाइड उनकी शारीरिक कठोरता, शक्ति और रासायनिक हमले के प्रतिरोध के लिए बहुत अधिक तापमान पर भी मूल्यवान हैं। आयरन कार्बाइड (सीमेंटाइट) स्टील और कच्चा लोहा का एक महत्वपूर्ण घटक है।
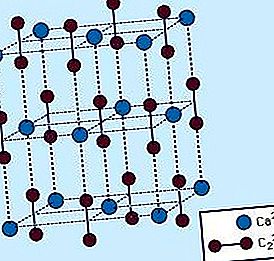
यूरेनियम प्रसंस्करण: कार्बाइड ईंधन
विभिन्न यूरेनियम और प्लूटोनियम कार्बाइड्स को जाना जाता है, जिसमें मोनोकारबाइड्स (यूसी, पीयूसी), सेस्काइकार्बाइड्स (यू 2 सी 3)
कार्बाइड की तैयारी
कार्बाइड कार्बन और इसी तरह के या निचले इलेक्ट्रोनगेटिविटी के एक तत्व से तैयार होते हैं, आमतौर पर या तो एक धातु या एक धातु ऑक्साइड होता है, 1,000-2,800 ° C (1,800–5,100 ° F) के तापमान पर। लगभग किसी भी कार्बाइड को कई सामान्य तरीकों में से एक द्वारा तैयार किया जा सकता है। पहली विधि में उच्च तापमान (2,000 ° C [3,600 ° F] या अधिक) पर तत्वों का प्रत्यक्ष संयोजन शामिल है। दूसरी विधि एक धातु के एक यौगिक की प्रतिक्रिया है, आमतौर पर एक ऑक्साइड, उच्च तापमान पर कार्बन के साथ। दो अतिरिक्त तरीकों में एक हाइड्रोकार्बन के साथ धातु या धातु नमक की प्रतिक्रिया शामिल होती है, आमतौर पर एसिटिलीन, सी 2 एच 2 । तरीकों में से एक में, गर्म धातु एक गैसीय हाइड्रोकार्बन के साथ प्रतिक्रिया करता है; दूसरे में, एक धातु को तरल अमोनिया, एनएच 3 में भंग कर दिया जाता है, और हाइड्रोकार्बन को समाधान के माध्यम से बुदबुदाया जाता है। एसिटिलीन के साथ तैयार किए गए कार्बाइड को एसिटाइलसाइड कहा जाता है और इसमें सी 2 2ion आयन होता है। उदाहरण के लिए, तरल अमोनिया में क्षार धातु को भंग करके और एसिटिलीन को समाधान के माध्यम से पारित करके क्षार धातु एसिटाइलाइड्स को सबसे अच्छा तैयार किया जाता है। इन यौगिकों, जिनमें सामान्य सूत्र एम 2 सी 2 (जहां एम धातु है), रंगहीन, क्रिस्टलीय ठोस हैं। वे पानी के साथ हिंसक प्रतिक्रिया करते हैं और जब हवा में गर्म होते हैं, तो कार्बोनेट को ऑक्सीकरण किया जाता है। क्षारीय-पृथ्वी कार्बाइड भी एसिटाइलाइड हैं। उनके पास सामान्य सूत्र MC 2 है और 500 ° C (900 ° F) से ऊपर एसिटिलीन के साथ क्षारीय-पृथ्वी धातु को गर्म करके तैयार किया जाता है।
कार्बाइड का वर्गीकरण
संरचनात्मक प्रकार के आधार पर कार्बाइड का वर्गीकरण मुश्किल है, लेकिन उनके गुणों में सामान्य रुझानों से तीन व्यापक वर्गीकरण उत्पन्न होते हैं। सबसे अधिक इलेक्ट्रोपोसिटिव धातुएं आयनिक या नमक की तरह के कार्बाइड बनाती हैं, आवर्त सारणी के मध्य में संक्रमण धातुएं बनती हैं, जिन्हें अंतरालीय कार्बाइड कहा जाता है, और कार्बन सहसंयोजक या आणविक कार्बाइड के समान इलेक्ट्रोनगेटिविटी के अधातु।
आयनिक कार्बाइड
आयनिक कार्बाइड में C 4− रूपों के कार्बन आयन होते हैं, जिन्हें कभी-कभी मिथेनाइड्स भी कहा जाता है क्योंकि उन्हें मीथेन, (CH 4) से प्राप्त किया जा सकता है; सी 2 2 from, एसिटिलाइड्स और एसिटिलीन से व्युत्पन्न कहा जाता है (सी 2 एच 2); और सी 3 4, से प्राप्त allene (सी 3 एच 4)। सबसे अच्छी तरह से चित्रित मेथनाइड संभवतः बेरिलियम कार्बाइड (बी 2 सी) और एल्यूमीनियम कार्बाइड (अल 4 सी 3) हैं। बेरिलियम ऑक्साइड (BeO) और कार्बन ईंट-रेड बेरिलियम कार्बाइड का उत्पादन करने के लिए 2,000 ° C (3,600 ° F) पर कार्बन प्रतिक्रिया करते हैं, जबकि एक भट्ठी में एल्यूमीनियम और कार्बन से पीला पीला एल्यूमीनियम कार्बाइड तैयार किया जाता है। एल्युमीनियम कार्बाइड एक सामान्य मीथेनाइड के रूप में पानी के साथ मीथेन के उत्पादन के लिए प्रतिक्रिया करता है। अल 4 सी 3 + 12 एच 2 ओ → 4 एएल (ओएच) 3 + 3CH 4
कई एसिटाइलाइड्स हैं जो अच्छी तरह से ज्ञात हैं और अच्छी तरह से विशेषता हैं। ऊपर वर्णित क्षार धातुओं और क्षारीय-पृथ्वी धातुओं के अलावा, लैंथेनम (ला) दो अलग-अलग एसिटलाइड, और तांबा (Cu), चांदी (Ag) और सोना (Au) रूप में विस्फोटक एसिटाइलाइड बनाता है। जस्ता (Zn), कैडमियम (Cd), और पारा (Hg) भी एसिटाइलाइड्स का निर्माण करते हैं, हालांकि वे भी समान नहीं हैं। इन यौगिकों में सबसे महत्वपूर्ण कैल्शियम कार्बाइड, सीएसी 2 है । कैल्शियम कार्बाइड के लिए प्राथमिक उपयोग रासायनिक उद्योग में उपयोग के लिए एसिटिलीन के स्रोत के रूप में है। कैल्शियम कार्बाइड को लगभग 2,200 ° C (4,000 ° F) पर कोक के रूप में कैल्शियम ऑक्साइड (चूना), CaO और कार्बन से औद्योगिक रूप से संश्लेषित किया जाता है। शुद्ध कैल्शियम कार्बाइड में उच्च गलनांक (2,300 ° C [4,200 ° F]) होता है और यह रंगहीन ठोस होता है। पानी के साथ सीएसी 2 की प्रतिक्रिया सी 2 एच 2 और गर्मी की एक महत्वपूर्ण मात्रा होती है, इसलिए प्रतिक्रिया सावधानीपूर्वक नियंत्रित परिस्थितियों में की जाती है। सीएओ + 3 सी → सीएसी 2 + सीओ
सीएसी 2 + 2 एच 2 ओ → सी 2 एच 2 + सीए (ओएच) 2 कैल्शियम कार्बाइड भी ऊंचे तापमान पर नाइट्रोजन गैस के साथ प्रतिक्रिया करता है (1,000-1,200 डिग्री सेल्सियस [1,800-2,200 ° F]) कैल्शियम सायनामाइड, CaCN 2 का निर्माण करें । सीएसी 2 + एन 2 → सीएसीएन 2 + सीटीआईएस एक महत्वपूर्ण औद्योगिक प्रतिक्रिया है क्योंकि सीएएनएन 2 एक उर्वरक के रूप में व्यापक उपयोग करता है, जो कि पानी के साथ अपनी प्रतिक्रिया के कारण साइनाइमाइड, एच 2 एनसीएन का उत्पादन करता है । अधिकांश MC 2 एसिटीलाइड्स में CaC 2 संरचना होती है, जो क्यूबिक सोडियम क्लोराइड (NaCl) संरचना से प्राप्त होती है। C 2 इकाइयाँ सेल अक्षों के साथ समानान्तर स्थित होती हैं, जिससे घन से चतुर्भुज तक कोशिका का विरूपण होता है।
इंटरस्टीशियल कार्बाइड्स
इंटरस्टीशियल कार्बाइड मुख्य रूप से अपेक्षाकृत बड़े संक्रमण धातुओं से प्राप्त होते हैं जो छोटे कार्बन परमाणुओं के लिए एक मेजबान जाली के रूप में कार्य करते हैं, जो करीब-पैक धातु के परमाणुओं के अंतर पर कब्जा कर लेते हैं। (क्रिस्टल को ठोस पदार्थों में पैक करने की व्यवस्था की चर्चा के लिए देखें।) इंटरस्टीशियल कार्बाइड्स की विशेषता अत्यधिक कठोरता है, लेकिन साथ ही साथ चरम भंगुरता भी है। उनके पास बहुत अधिक गलनांक होता है (आमतौर पर लगभग 3,000-4,000 ° C [5,400–7,200 ° F]) और धातु से जुड़े कई गुणों को बनाए रखते हैं, जैसे कि ऊष्मा और विद्युत की उच्च चालकता और साथ ही धात्विक चमक। ऊंचे तापमान पर कुछ अंतरालीय कार्बाइड धातुओं के यांत्रिक गुणों को बनाए रखते हैं, जैसे कि मॉलबिलिटी। प्रारंभिक संक्रमण धातुओं में से कई में रेडी होते हैं जो इंटरस्टीशियल मोनोकारबाइड्स, एमसी बनाने के लिए पर्याप्त बड़े होते हैं। महत्वपूर्ण (यानी, न्यूनतम) त्रिज्या लगभग 1.35 एंगस्ट्रॉम (1.35 × 10 cm8 सेमी, या 5.32 × 10 inch9 इंच) प्रतीत होती है । हालांकि, अधिकांश संक्रमण धातु कई स्टोइकियोमेट्री के अंतरालीय कार्बाइड बनाते हैं। उदाहरण के लिए, मैंगनीज (एमएन) को कम से कम पांच अलग-अलग अंतरालीय कार्बाइड बनाने के लिए जाना जाता है। आयनिक कार्बाइड के विपरीत, अधिकांश अंतरालीय कार्बाइड पानी के साथ प्रतिक्रिया नहीं करते हैं और रासायनिक रूप से निष्क्रिय हैं। टंगस्टन कार्बाइड (WC) और टैंटलम कार्बाइड (TaC) सहित कई औद्योगिक महत्व हैं, जो अपनी अत्यधिक कठोरता और रासायनिक जड़ता के कारण उच्च गति वाले काटने के उपकरण के रूप में उपयोग किए जाते हैं। स्टील में आयरन कार्बाइड (सीमेंटाइट), फे 3 सी, एक महत्वपूर्ण घटक है।






![एंग्लो-आयरिश समझौता यूनाइटेड किंगडम-आयरलैंड [1985] एंग्लो-आयरिश समझौता यूनाइटेड किंगडम-आयरलैंड [1985]](https://images.thetopknowledge.com/img/politics-law-government/2/anglo-irish-agreement-united-kingdom-ireland-1985.jpg)