मानक अमीनो एसिड
सबसे उपयोगी शिष्टाचार में से एक जिसके द्वारा मानक (या आम) अमीनो एसिड को वर्गीकृत करने के लिए आर समूह (जैसे, साइड चेन) के ध्रुवता (विद्युत आवेश का वितरण) पर आधारित है।
समूह I: नॉनपोलर अमीनो एसिड
समूह I एमिनो एसिड ग्लाइसिन, ऐलेनिन, वेलीन, ल्यूसीन, आइसोल्यूसिन, प्रोलाइन, फेनिलएलनिन, मेथिओनिन और ट्रिप्टोफैन हैं। इन अमीनो एसिड के आर समूहों में या तो स्निग्ध या सुगंधित समूह होते हैं। यह उन्हें हाइड्रोफोबिक ("पानी से डर") बनाता है। जलीय घोलों में, गोलाकार प्रोटीन प्रोटीन के आंतरिक भाग में इन हाइड्रोफोबिक पक्ष श्रृंखलाओं को दफनाने के लिए तीन आयामी आकार में बदल जाएगा। समूह I एमिनो एसिड की रासायनिक संरचनाएं हैं:
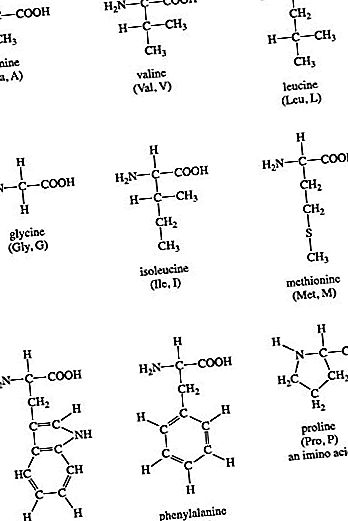
Isoleucine ल्यूकोइन का एक आइसोमर है, और इसमें दो चिरल कार्बन परमाणु होते हैं। प्रोलिन मानक अमीनो एसिड के बीच अद्वितीय है क्योंकि इसमें मुक्त α-amino और मुक्त α-carboxyl समूह दोनों नहीं हैं। इसके बजाय, इसकी साइड चेन एक चक्रीय संरचना बनाती है क्योंकि प्रोलाइन का नाइट्रोजन परमाणु दो कार्बन परमाणुओं से जुड़ा हुआ है। (कड़ाई से बोलते हुए, इसका मतलब है कि प्रोलिन एक एमिनो एसिड नहीं है, बल्कि एक α-imino एसिड है।) फेनिलएलनिन, जैसा कि नाम से पता चलता है, इसमें एलेनिन से जुड़ा एक फिनाइल समूह होता है। मेथियोनीन दो अमीनो एसिड में से एक है जिसमें सल्फर परमाणु होता है। मेथिओनिन प्रोटीन बायोसिंथेसिस (अनुवाद) में एक केंद्रीय भूमिका निभाता है क्योंकि यह लगभग हमेशा अमीनो एसिड की शुरुआत है। मेथिओनिन चयापचय के लिए मिथाइल समूह भी प्रदान करता है। ट्रिप्टोफैन में एक इंडोल रिंग होती है जो कि अलनील साइड चेन से जुड़ी होती है।
समूह II: ध्रुवीय, अपरिवर्तित अमीनो एसिड
समूह II अमीनो एसिड सेरीन, सिस्टीन, थ्रेओनीन, टायरोसिन, शतावरी, और ग्लोसामाइन हैं। इस समूह में साइड चेन के पास कार्यात्मक समूहों का एक स्पेक्ट्रम है। हालांकि, अधिकांश में पानी और अन्य अणुओं के लिए हाइड्रोजन बंधन के लिए उपलब्ध इलेक्ट्रॉन जोड़े के साथ कम से कम एक परमाणु (नाइट्रोजन, ऑक्सीजन या सल्फर) होता है। समूह II अमीनो एसिड की रासायनिक संरचनाएं हैं:

दो अमीनो एसिड, सेरीन और थ्रेओनीन, एलिफैटिक हाइड्रॉक्सिल समूह होते हैं (यानी, हाइड्रोजन परमाणु एक हाइड्रोजन परमाणु से बंधा होता है, जिसे)OH के रूप में दर्शाया जाता है)। टायरोसिन में एरोमैटिक रिंग में एक हाइड्रॉक्सिल समूह होता है, जो इसे फिनोल व्युत्पन्न बनाता है। इन तीन अमीनो एसिड में हाइड्रॉक्सिल समूह एक महत्वपूर्ण प्रकार के पोस्टट्रांसलैशनल संशोधन के अधीन हैं: फॉस्फोरिलीकरण (गैरमानक अमीनो एसिड नीचे देखें)। मेथियोनीन की तरह, सिस्टीन में एक सल्फर परमाणु होता है। मेथियोनीन के सल्फर परमाणु के विपरीत, हालांकि, सिस्टीन का सल्फर रासायनिक रूप से प्रतिक्रियाशील है (सिस्टीन ऑक्सीकरण के नीचे देखें)। शतावरी, पहले शतावरी से अलग, और ग्लूटामाइन दोनों में आर समूह होते हैं। कार्बोनिल समूह हाइड्रोजन बांड स्वीकर्ता के रूप में कार्य कर सकता है, और अमीनो समूह (एनएच 2) हाइड्रोजन बांड दाता के रूप में कार्य कर सकता है।
समूह III: अम्लीय अमीनो एसिड
इस समूह के दो अमीनो एसिड एसपारटिक एसिड और ग्लूटामिक एसिड हैं। प्रत्येक की साइड चेन पर एक कार्बोक्जिलिक एसिड होता है जो इसे अम्लीय (प्रोटॉन-दान) गुण प्रदान करता है। शारीरिक पीएच में एक जलीय घोल में, इन अमीनो एसिड पर सभी तीन कार्यात्मक समूह आयनीकृत करेंगे, इस प्रकार −1 का समग्र प्रभार देंगे। आयनिक रूपों में, अमीनो एसिड को एस्पार्टेट और ग्लूटामेट कहा जाता है। समूह III अमीनो एसिड की रासायनिक संरचनाएं हैं

एस्पार्टेट और ग्लूटामेट की साइड चेन आयनिक बॉन्ड ("नमक पुल") बना सकती हैं, और वे हाइड्रोजन बॉन्ड स्वीकर्स के रूप में भी कार्य कर सकते हैं। कई प्रोटीन जो संरचनात्मक या कार्यात्मक उद्देश्यों के लिए धातु आयनों ("मेटालोप्रोटीन") को बांधते हैं, उनके पास एस्पार्टेट या ग्लूटामेट साइड चेन या दोनों में धातु-बाध्यकारी साइटें होती हैं। मुक्त ग्लूटामेट और ग्लूटामाइन अमीनो एसिड चयापचय में एक केंद्रीय भूमिका निभाते हैं। ग्लूटामेट केंद्रीय तंत्रिका तंत्र में सबसे प्रचुर मात्रा में उत्तेजक न्यूरोट्रांसमीटर है।






![एंग्लो-आयरिश समझौता यूनाइटेड किंगडम-आयरलैंड [1985] एंग्लो-आयरिश समझौता यूनाइटेड किंगडम-आयरलैंड [1985]](https://images.thetopknowledge.com/img/politics-law-government/2/anglo-irish-agreement-united-kingdom-ireland-1985.jpg)