लोचदार गुण
जैसा कि दुर्लभ-पृथ्वी धातुओं के अन्य गुणों में से अधिकांश के साथ होता है, दुर्लभ-पृथ्वी धातुओं का लोचदार मापांक अन्य धातु तत्वों के मध्य प्रतिशतक में होता है। स्कैंडियम और yttrium के लिए मान उसी के बारे में हैं जैसे कि लैंथेनाइड्स के अंत सदस्य (एरबियम से लुटेटियम)। लोचदार संख्या में वृद्धि परमाणु संख्या के साथ एक सामान्य वृद्धि है। सेरियम (कुछ 4f संबंध) और ytterbium (divalency) के लिए विषम मूल्य स्पष्ट हैं।
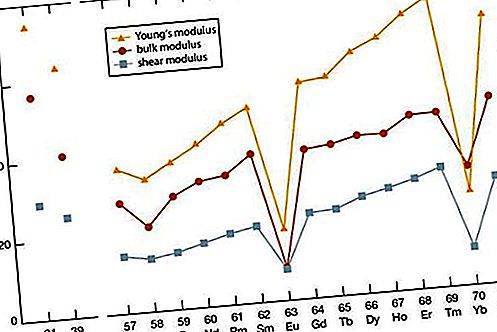
यांत्रिक विशेषताएं
दुर्लभ-पृथ्वी धातुएं न तो कमजोर हैं और न ही विशेष रूप से मजबूत धातु तत्व हैं, और वे कुछ मामूली लचीलापन दिखाते हैं। क्योंकि यांत्रिक गुण धातुओं की शुद्धता और उनके थर्मल इतिहास पर काफी निर्भर हैं, इसलिए साहित्य में कथित मूल्यों की तुलना करना मुश्किल है। परम शक्ति लगभग 120 से 160 एमपीए (मेगापैस्कल्स) और लगभग 15 से 35 प्रतिशत तक लचीलापन है। Ytterbium (युरोपियम को मापा नहीं गया है) की ताकत बहुत छोटी है, 58 एमपीए, और लचीलापन अधिक है, लगभग 45 प्रतिशत है, जैसा कि डायवलेंट धातु के लिए अपेक्षित होगा।
रासायनिक गुण
हवा के साथ दुर्लभ-पृथ्वी धातुओं की प्रतिक्रिया प्रकाश लैंथेनाइड और भारी के बीच एक महत्वपूर्ण अंतर दर्शाती है। हल्के लैंथेनाइड्स भारी लैंथेनाइड्स (लुटेटियम के माध्यम से गडोलिनियम), स्कैंडियम और यट्रियम की तुलना में बहुत अधिक तेजी से ऑक्सीकरण करते हैं। इस अंतर का गठन ऑक्साइड उत्पाद की भिन्नता के कारण होता है। प्रकाश लैंथेनाइड्स (नियोडिमियम के माध्यम से लैंथेनम) हेक्सागोनल ए-टाइप आर 2 ओ 3 संरचना बनाते हैं; मध्य लैंथेनाइड्स (गैडोलिनियम के माध्यम से समैरियम) मोनोक्लिनिक बी-टाइप आर 2 ओ 3 चरण का निर्माण करते हैं; जबकि भारी लैंथेनाइड्स, स्कैंडियम और येट्रियम क्यूबिक C-टाइप R 2 O 3 संशोधन करते हैं। ए-प्रकार हवा में जल वाष्प के साथ प्रतिक्रिया करता है जिससे एक ऑक्सीहाइड्रॉक्साइड बनता है, जो सफेद कोटिंग को फैलाने का कारण बनता है और ताजी धातु की सतह को उजागर करके ऑक्सीकरण को आगे बढ़ने की अनुमति देता है। सी-प्रकार ऑक्साइड एक तंग, सुसंगत कोटिंग बनाता है जो एल्यूमीनियम के व्यवहार के समान आगे ऑक्सीकरण को रोकता है। समैरियम और गैडोलीनियम, जो बी-टाइप आर 2 ओ 3 चरण बनाते हैं, भारी लैंथेनाइड्स, स्कैंडियम और येट्रियम की तुलना में थोड़ा तेज ऑक्सीकरण करते हैं, लेकिन फिर भी एक सुसंगत कोटिंग बनाते हैं जो आगे ऑक्सीकरण को रोकता है। इस वजह से, प्रकाश लैंथेनाइड्स को वैक्यूम या एक अक्रिय गैस वातावरण में संग्रहित किया जाना चाहिए, जबकि भारी लैंथेनाइड्स, स्कैंडियम और येट्रियम को बिना ऑक्सीकरण के वर्षों तक खुली हवा में छोड़ा जा सकता है।
यूरोपियम धातु, जिसमें एक बीसीसी संरचना होती है, नम हवा के साथ किसी भी दुर्लभ पृथ्वी के सबसे तेजी से ऑक्सीकरण करती है और एक अक्रिय गैस वातावरण में हर समय नियंत्रित करने की आवश्यकता होती है। युरोपियम की प्रतिक्रिया उत्पाद जब नम हवा के संपर्क में होता है, तो एक हाइड्रेट हाइड्रॉक्साइड होता है, Eu (OH) 2 ―H 2 O, जो एक असामान्य प्रतिक्रिया उत्पाद है क्योंकि अन्य सभी दुर्लभ-पृथ्वी धातुएं एक ऑक्साइड बनाती हैं।
धातुएं हाइड्रोफ्लोरिक एसिड (एचएफ) को छोड़कर सभी एसिड के साथ सख्ती से प्रतिक्रिया करती हैं, एच 2 गैस जारी करती हैं और इसी दुर्लभ-पृथ्वी-आयन यौगिक का निर्माण करती हैं। हाइड्रोफ्लोरिक एसिड में रखे जाने पर दुर्लभ-पृथ्वी धातु एक अघुलनशील आरएफ 3 कोटिंग बनाती है जो आगे की प्रतिक्रिया को रोकती है।
दुर्लभ-पृथ्वी की धातुएं आसानी से आरएच 2 बनाने के लिए हाइड्रोजन गैस के साथ प्रतिक्रिया करती हैं और मजबूत हाइड्राइडिंग परिस्थितियों में, आरएच 3 चरण - स्कैंडियम को छोड़कर, जो ट्राइहाइड्राइड नहीं बनाती है।
यौगिकों
दुर्लभ-पृथ्वी तत्व, सभी तत्वों के साथ हजारों यौगिकों का निर्माण करते हैं - और आवर्त सारणी में समूह 7 धातु (मैंगनीज, टेक्नेटियम, और रेनियम) सहित प्लस यौगिक बेरिलियम और मैग्नीशियम, जो दूर पर स्थित हैं समूह में बायां हाथ 2. महत्वपूर्ण यौगिक श्रृंखला और अद्वितीय गुणों या असामान्य व्यवहार वाले कुछ व्यक्तिगत यौगिक नीचे वर्णित हैं।
आक्साइड
अकार्बनिक दुर्लभ-पृथ्वी यौगिकों का सबसे बड़ा परिवार आज तक अध्ययन किया गया है। सबसे आम stoichiometry R 2 O 3 संयोजन है, लेकिन, क्योंकि कुछ लैंथेनाइड तत्वों में 3 + के अलावा अन्य वैलेंस स्टेट्स भी हैं, अन्य stoichiometries मौजूद हैं - उदाहरण के लिए, सेरियम ऑक्साइड (CeO 2), प्रेडोडायमियम ऑक्साइड (Pr 6 O 11)), टेरबियम ऑक्साइड (Tb 4 O 7), यूरोपियम ऑक्साइड (EuO), और Eu 3 O 4 । अधिकांश चर्चा बाइनरी ऑक्साइड पर केंद्रित होगी, लेकिन टर्नरी और अन्य उच्च-क्रम ऑक्साइड की भी संक्षिप्त समीक्षा की जाएगी।













