पॉलीवलेंट सल्फर के कार्बनिक यौगिक: सल्फोऑक्साइड और सल्फोन
ऑर्गेनोसल्फर यौगिकों के दो प्रमुख समूह जिनके पास कार्बनिक ऑक्सीजन यौगिकों के बीच कोई समकक्ष नहीं है, वे हैं सल्फॉक्साइड्स और सल्फोन्स। अगर इन यौगिकों में बंध को दोगुना बंधुआ संरचनाओं के साथ दर्शाया जाता है - जैसे, (S (= O) - सल्फोक्साइड के लिए और oxS (= O) 2 - सल्फोने के लिए - सल्फर परमाणु क्रमशः "देखें" 10 और 12 वाल्व इलेक्ट्रॉन। यह ऑक्टेट नियम की अनुमति से अधिक है, लेकिन सल्फर ऑक्टेट नियम से बाध्य नहीं है, क्योंकि यह इसकी बॉन्डिंग में 3 डी ऑर्बिटल्स का उपयोग कर सकता है, क्योंकि सल्फर हेक्साफ्लोराइड (एसएफ 6) जैसे यौगिकों में भी आवश्यक होगा)। जबकि आठ से अधिक इलेक्ट्रॉनों को समायोजित करने के लिए सल्फर वैलेंस शेल के विस्तार के लिए कुछ सैद्धांतिक समर्थन है, बॉन्डिंग योजनाओं में 3 डी ऑर्बिटल्स के उपयोग की आलोचना की गई है क्योंकि 3 डी ऑर्बिटल्स सल्फर 3 एस और 3 पी ऑर्बिटल्स की तुलना में ऊर्जा में बहुत अधिक हैं। एक वैकल्पिक बॉन्डिंग मॉडल सल्फ़ोक्साइड के लिए (S + (--O -) - जैसे oxS + और ―S 2+ (--O -) 2− के लिए ध्रुवीय संबंध बनाता है। हालांकि यह स्पष्ट है कि ध्रुवीय अनुनाद संरचना समग्र संबंध में योगदान करती है, यह संभव है कि सल्फर 3 डी ऑर्बिटल्स से भी कुछ योगदान हो। यह ध्यान दिया जाना चाहिए कि सल्फॉक्साइड समूह में सल्फर परमाणु पर इलेक्ट्रॉनों की एक अकेली जोड़ी भी होती है, जिसके लिए आवश्यक है कि सल्फॉक्साइड समूह एक अमाइन के समान नॉनप्लेनर हो, लेकिन कार्बोनिल समूह के प्लानर संरचना से काफी अलग, ―C (= O)) -, जिसके लिए कभी-कभी एक सल्फोऑक्साइड समूह की तुलना की जाती है। सल्फोक्साइड समूह की नॉनप्लानैरिटी का एक महत्वपूर्ण परिणाम यह है कि टाइप R (S = O) R O, जहां R और R, अलग हैं, के सल्फोक्साइड, चिरल हैं और वास्तव में ऑप्टोन सक्रिय रूप में अलग किए जा सकते हैं, जिसमें सल्फोने समूह होता है। टेट्राहेड्रल होना। एमाइन के विपरीत, लेकिन फॉस्फिन के समान, ट्राइकोर्डिनेट सल्फर (तीन लिगेंड के साथ ट्राइकोनल पिरामिडल सल्फर कंपाउंड और सल्फर पर इलेक्ट्रॉनों की एक अकेली जोड़ी-जैसा कि उदाहरण के लिए, सल्फिनिन क्लोराइड, सल्फाइट एस्टर, सल्फोक्साइड, थायोसल्फेट, और सल्फिलिमाइन) में है। स्थिर विन्यास, सल्फर (कम भीड़) के लिए लंबे समय तक बांड और लोन पेयर एस-कैरेक्टर की अधिक मात्रा (संकरण में उपयोग की जाने वाली ऑर्बिटल्स की कुल संख्या का प्रतिशत)। कई वैकल्पिक रूप से सक्रिय ट्राइकोर्डिनेट यौगिक प्रकृति में होते हैं, और वैकल्पिक रूप से सक्रिय सल्फर यौगिकों को व्यापक रूप से अन्य चिरल यौगिकों के संश्लेषण में उपयोग किया जाता है।
सल्फॉक्साइड्स का नामकरण केवल वर्णमाला के क्रम में किया जाता है, attachedS (= O) - समूह से जुड़े दो कार्बनिक समूह, जिसके बाद सल्फोक्साइड शब्द होता है (उदाहरण के लिए, इथाइल मिथाइल सल्फ़ोक्साइड, CH 3 S (O) C 2 H 5), या कण-सल्फिनिल- (जैसे, 4- (मिथाइलसल्फिनिल) बेंजोइक एसिड) का उपयोग करके समूहों के सरल नाम से एक उपसर्ग बनाकर। सल्फोन्स का नामकरण सल्फोक्साइड के समान है; कण -sulfonyl- का उपयोग जटिल मामलों में किया जाता है। अधिकांश सल्फ़ॉक्साइड रंगहीन तरल पदार्थ या कम पिघलने वाले बिंदुओं के साथ ठोस होते हैं। कम आणविक भार वाले सल्फोऑक्साइड डिमिथाइल सल्फोऑक्साइड (CH 3 S (= O) CH 3, DMSO) पानी में घुलनशील है, कम विषाक्तता प्रदर्शित करता है, और एक उत्कृष्ट विलायक है। यह तेजी से त्वचा में घुसने की असामान्य क्षमता रखता है और इस तरह से त्वचा के माध्यम से यौगिकों को ले जा सकता है। पशु चिकित्सा में इसका कुछ उपयोग है, विशेष रूप से घोड़ों में लंगड़ापन के इलाज में। सल्फास आमतौर पर रंगहीन क्रिस्टलीय ठोस होते हैं। डाइमेथाइल सल्फोन पानी में घुलनशील है। डायरिल सल्फोन (pH 2 NC 6 H 4 SO 2 C 6 H 4 NH 2 -p; उदा। Dapsone) और संबंधित यौगिकों का उपयोग तपेदिक और कुष्ठ रोग के उपचार में किया गया है। पॉलीसल्फोन रेजिन, जो एक बहुलक के भीतर CSO 2 C 6 H 4 - इकाई को शामिल करते हैं, का उपयोग विद्युत और ऑटोमोटिव भागों और अन्य अनुप्रयोगों के लिए बड़े पैमाने पर किया जाता है, जिसमें उत्कृष्ट थर्मल स्थिरता और ऑक्सीकरण के प्रतिरोध की आवश्यकता होती है।
घटना और तैयारी
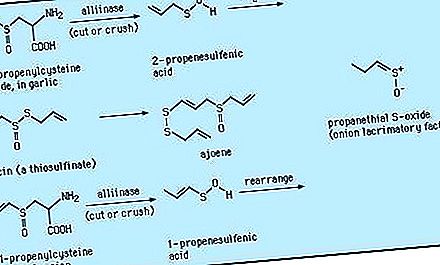
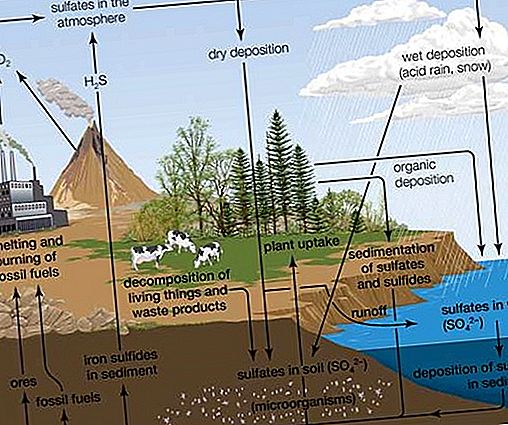
प्राकृतिक स्रोतों से पृथक किए गए यौगिकों में, एस-एल्काइल सिस्टीन एस-ऑक्साइड (जैसे एस -1 और एस -2 प्रोपेलेनिसिस्टीन एस-ऑक्साइड) - जीनस एलियम के पौधों के पुष्पक्रमों के अग्रदूत पहले पाए गए थे कार्बन के साथ-साथ एक अन्य तत्व (सल्फर) में ऑप्टिकल गतिविधि। ब्रोकोली से सल्फोराफेन (सीएच 3 एस (ओ) (सीएच 2) 4 एनसीएस) सहित प्राकृतिक स्रोतों से कई अन्य सल्फोनोक्साइड अलग-अलग हो गए हैं, जो ट्यूमर के विकास को रोकते हैं, और प्याज के अर्क से ज़्विलीबेलनेस की सूचना देते हैं। डीएमएसओ व्यापक रूप से तीन भागों प्रति मिलियन (पीपीएम) या उससे कम के स्तर पर पाया जाता है और यह समुद्री जल सहित प्राकृतिक जल का एक सामान्य घटक है। डिमेथाइल सल्फोन के साथ, डीएमएसओ का उत्पादन अल्गल चयापचय के माध्यम से किया जा सकता है। बारिश के पानी में पाए जाने पर, DMSO वायुमंडलीय डाइमेथाइल सल्फाइड, (CH 3) 2 S के ऑक्सीकरण से उत्पन्न हो सकता है, जो वैश्विक सल्फर चक्र में जैविक मूल के सल्फर के प्राकृतिक हस्तांतरण के हिस्से के रूप में होता है।
सल्फाइड के सल्फाइड के ऑक्सीकरण द्वारा सोडियम मेटापेरियोडेट (NaIO 4) या हाइड्रोजन पेरोक्साइड (H 2 O 2) के साथ आसानी से तैयार किया जाता है । व्यावसायिक रूप से, डीएमएसओ को डाइमिथाइल सल्फाइड के वायु / नाइट्रिक ऑक्साइड-उत्प्रेरित ऑक्सीकरण से बनाया गया है, जो कागज के निर्माण के लिए क्राफ्ट सल्फेट प्रक्रिया का एक प्रमुख उप-उत्पाद है। सल्फाइड्स या सल्फोक्साइड्स का अधिक-जोरदार ऑक्सीकरण, उदाहरण के लिए, पोटेशियम परमैंगनेट के साथ, KMnO 4 - सल्फाइड्स का उत्पादन करता है । वैकल्पिक रूप से सक्रिय सल्फॉक्साइड्स को आरएसआर of के सल्फाइड के ऑक्सीकरण द्वारा तैयार किया जा सकता है, जहां आर ′ आर ants, वैकल्पिक रूप से सक्रिय ऑक्सीडेंट या सूक्ष्मजीवविज्ञानी ऑक्सीडेंट के साथ। वैकल्पिक रूप से, वैकल्पिक रूप से सक्रिय सल्फोक्साइड्स को वैकल्पिक रूप से सक्रिय सल्फिनिल डेरिवेटिव्स आरएस (= ओ) एक्स, जहां एक्स = ओ, एन, या एस, रिएलिटी या आरएमजीबीआर जैसे अभिकर्मकों के साथ तैयार किया जा सकता है। सॉल्वेंट सल्फ़ोलेन (थिओलेन एस, एस-डाइऑक्साइड) पहले सल्फर डाइऑक्साइड के साथ प्रतिक्रिया करता है, जिसमें सल्फ़ोलीन (एक चक्रीय, असंतृप्त, पाँच-सदस्यीय रिंग सल्फ़ोन) देने के लिए ब्यूटाडीन के साथ सल्फर डाइऑक्साइड की प्रतिक्रिया होती है।

सुगंधित हाइड्रोकार्बन के साथ सल्फोनील क्लोराइड की प्रतिक्रिया से सुगंधित सल्फोन्स भी बनाया जा सकता है। थायोफिन एस-ऑक्साइड और एस, एस-डाइऑक्साइड, थायोफिनेस के ऑक्सीकरण से बनते हैं, माता-पिता थियोफिनेस की तुलना में कहीं अधिक प्रतिक्रियाशील होते हैं क्योंकि ऑक्सीजन द्वारा सल्फर पर इलेक्ट्रॉनों के एक या दोनों जोड़े के प्रतिस्थापन के परिणामस्वरूप सुगंधित होने के नुकसान।













![जंगल की लड़ाई अमेरिकी नागरिक युद्ध [1864] जंगल की लड़ाई अमेरिकी नागरिक युद्ध [1864]](https://images.thetopknowledge.com/img/world-history/0/battle-wilderness-american-civil-war-1864.jpg)