नियोडिमियम (एनडी), रासायनिक तत्व, आवर्त सारणी के लैंथेनाइड श्रृंखला की एक दुर्लभ-पृथ्वी धातु।
नियोडिमियम एक नमनीय और निंदनीय सफेद धातु है। यह आसानी से हवा में ऑक्सीकरण करता है, एक ऑक्साइड बनाता है, एनडी 2 ओ 3, जो आसानी से स्पॉल करता है, धातु को आगे ऑक्सीकरण के लिए उजागर करता है। धातु को एक प्लास्टिक कवर में सील करके या वैक्यूम या निष्क्रिय वातावरण में रखा जाना चाहिए। यह खनिज एसिड के साथ धीरे-धीरे प्रतिक्रिया करता है - हाइड्रोफ्लोरिक एसिड (एचएफ) को छोड़कर, जिसमें यह ट्राइफ्लोराइड, एनडीएफ 3 की एक सुरक्षात्मक परत बनाता है । Neodymium दृढ़ता से पैरामैग्नेटिक है और 7.5 और 19.9 K (−265.7 और.7253.3 ° C, या par446.2 और −423.9 ° F) पर अलग-अलग स्वतंत्र साइटों, हेक्सागोनल और क्यूबिक पर अलग-अलग विकसित होने वाले सहज चुंबकीय क्षणों के साथ आदेश देता है।
ऑस्ट्रियाई रसायनशास्त्री कार्ल एयूआर वॉन वेलस्बैक ने 1885 में डायोडिया (दुर्लभ पृथ्वी के आक्साइड का मिश्रण) से तैयार अमोनियम डाइडियम नाइट्रेट को एक नियोडिमियम अंश और एक प्रोडोडाइमियम अंश में दोहराया क्रिस्टलीकरण द्वारा अलग किया। दुर्लभ पृथ्वी में से केवल योड्रियम, लैंटानम और सेरियम, नियोडिमियम की तुलना में अधिक बहुतायत से हैं। पृथ्वी की पपड़ी के आग्नेय चट्टानों में, यह सीसे की तुलना में दोगुना और तांबे के रूप में बहुतायत से लगभग आधा है।
प्राकृतिक नियोडिमियम सात विभिन्न समस्थानिकों का मिश्रण है। उनमें से पांच स्थिर हैं- नियोडिमियम -142 (27.13 प्रतिशत), नियोडिमियम -148 (17.19 प्रतिशत), नियोडिमियम -143 (12.18 प्रतिशत), नियोडिमियम -148 (8.30 प्रतिशत), और नियोडिमियम -148 (5.76 प्रतिशत) - और दो दो हैं रेडियोधर्मी, नियोडिमियम -144 (23.80 प्रतिशत) और नियोडिमियम -150 (5.64 प्रतिशत)। नियोडिमियम (परमाणु समस्थानिकों को छोड़कर) के कुल 31 रेडियोधर्मी समस्थानिकों की विशेषता रही है, जिनका द्रव्यमान 124 से 161 तक और अर्ध-जीवन में 0.65 सेकेंड (नियोडिमियम -125) से 7.9 × 10 18 वर्ष (नियोडिमियम -150) तक है।
Neodymium खनिज monazite और bastnasite में होता है और परमाणु विखंडन का एक उत्पाद है। तरल-तरल पृथक्करण या आयन-विनिमय तकनीकों को नियोडिमियम के पृथक्करण और शुद्धिकरण के लिए नियोजित किया जाता है। धातु खुद को जुड़े हुए हिस्सों के इलेक्ट्रोलिसिस द्वारा या कैल्शियम के साथ फ्लोराइड की मेटालोथर्मिक कमी से तैयार किया जाता है। नियोडिमियम के दो अलॉट्रोपेस (संरचनात्मक रूप) मौजूद हैं: α- चरण डबल क्लोज-पैक हेक्सागोनल है जिसमें कमरे के तापमान पर = 3.6582 Å और c = 11.7966 (है। The-चरण 883 ° C (1,621 ° F) पर = 4.13 is के साथ शरीर-केंद्रित घन है।
नियोडायमियम का प्रमुख अनुप्रयोग एनडी 2 फीट 14 बी पर आधारित उच्च शक्ति वाले स्थायी मैग्नेट में है जो उच्च प्रदर्शन वाले इलेक्ट्रिक मोटर्स और जनरेटर में उपयोग किया जाता है, साथ ही कंप्यूटर हार्ड ड्राइव और विंड टर्बाइन के लिए स्पिंडल मैग्नेट में भी होता है। धातु का उपयोग इलेक्ट्रॉनिक्स उद्योग में किया जाता है, स्टील के निर्माण में और घटक के रूप में कई लौह और गैर-लौह मिश्र धातुओं के बीच, उनमें से मिच धातु (15 प्रतिशत neodymium), का उपयोग हल्के फ्लेक्स के लिए किया जाता है। धातु ही- और मिश्र धातु के रूप में एक अन्य लैंथेनाइड के साथ, एर्बियम - को 4.2 K (9269 ° C, या 2452 F F) तक ठंडा करने के लिए निम्न-तापमान क्रायोकूलर अनुप्रयोगों में एक पुनर्योजी के रूप में नियोजित किया गया है। इसके यौगिकों का उपयोग सिरेमिक उद्योग में ग्लेज़ के लिए और गुलाबी से बैंगनी तक विभिन्न रंगों में कांच को रंगने के लिए किया जाता है। नियोडिमियम-स्टेबिलाइज्ड येट्रियम एल्युमिनियम गार्नेट (YAG) कई आधुनिक लेजर का एक घटक है, और फाइबर ऑप्टिक्स में नियोडिमियम ग्लास का उपयोग किया जाता है। नियोडायमियम और प्रेज़ोडियम का मिश्रण हानिकारक सोडियम-डी वर्णक्रमीय रेखाओं के क्षेत्र में प्रकाश को अवशोषित करता है और इसलिए वेल्ड के ग्लास और ग्लासब्लोवर्स के चश्मे में उपयोग किया जाता है।
ऑक्साइड एनडी 2 ओ 3 और हाइड्रॉक्साइड एनडी (ओएच) 3 जैसे इसके यौगिकों में तत्व लगभग हमेशा +3 ऑक्सीकरण अवस्था में होता है; एनडी 3+ आयन पानी में स्थिर है। +2 राज्य में नियोडायमियम के केवल कुछ यौगिक तैयार किए गए हैं, जैसे कि डायोडाइड एनडीआई 2 और डाइक्लोराइड एनडीसीएल 2; एनडी 2+ आयन जलीय घोल में अस्थिर है।
तत्व गुण
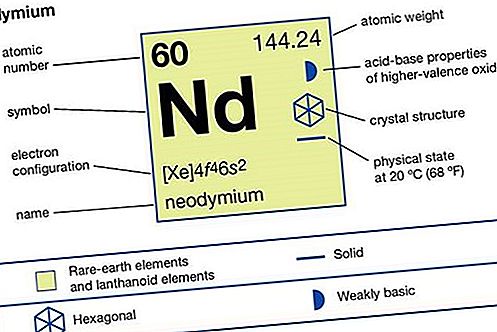
| परमाणु क्रमांक | 60 |
|---|---|
| परमाण्विक भार | 144.24 |
| गलनांक | 1,021 ° C (1,870 ° F) |
| क्वथनांक | 3,074 ° C (5,565 ° F) |
| विशिष्ट गुरुत्व | 7.008 (25 ° C, या 77 ° F) |
| ऑक्सीकरण स्थिति | +2 (दुर्लभ, अस्थिर), +3 |
| ऋणावेशित सूक्ष्म अणु का विन्यास | [Xe] 4f 4 6s 2 |










![रोम यूरोप की संधि [1957] रोम यूरोप की संधि [1957]](https://images.thetopknowledge.com/img/politics-law-government/1/treaty-rome-europe-1957.jpg)

