यूरेनियम प्रसंस्करण, विभिन्न उत्पादों में उपयोग के लिए अयस्क की तैयारी।
यूरेनियम (U), हालांकि बहुत घना (19.1 ग्राम प्रति क्यूबिक सेंटीमीटर), अपेक्षाकृत कमजोर, अपरिष्कृत धातु है। दरअसल, यूरेनियम के धात्विक गुण चांदी और अन्य वास्तविक धातुओं और अधातु तत्वों में से एक के बीच मध्यवर्ती प्रतीत होते हैं, ताकि यह संरचनात्मक अनुप्रयोगों के लिए मूल्यवान न हो। यूरेनियम का प्रमुख मूल्य इसके समस्थानिकों के रेडियोधर्मी और विखंडनीय गुणों में है। प्रकृति में, धातु के लगभग सभी (99.27 प्रतिशत) में यूरेनियम -238; शेष में यूरेनियम -235 (0.72 प्रतिशत) और यूरेनियम -234 (0.006 प्रतिशत) शामिल हैं। स्वाभाविक रूप से होने वाले समस्थानिकों में से, केवल यूरेनियम -235 न्यूट्रॉन विकिरण द्वारा सीधे विखंडनीय है। हालाँकि, यूरेनियम -238, एक न्यूट्रॉन को अवशोषित करने पर, यूरेनियम -239 बनाता है, और यह बाद के आइसोटोप अंततः प्लूटोनियम -239 में परमाणु ऊर्जा और परमाणु हथियारों में बहुत महत्व का एक फ़िसाइल सामग्री बन जाता है। एक अन्य फिसाइल आइसोटोप, यूरेनियम -233, थोरियम -232 के न्यूट्रॉन विकिरण द्वारा बनाया जा सकता है।
यहां तक कि कमरे के तापमान पर, ऑक्सीजन और नाइट्रोजन के साथ सूक्ष्मता से विभाजित यूरेनियम धातु प्रतिक्रिया करता है। उच्च तापमान पर यह इंटरलामेटिक यौगिक बनाने के लिए विभिन्न प्रकार के मिश्र धातु धातुओं के साथ प्रतिक्रिया करता है। अन्य धातुओं के साथ ठोस-घोल का निर्माण केवल शायद ही कभी होता है, यूरेनियम परमाणुओं द्वारा गठित एकवचन क्रिस्टलीय संरचनाओं के कारण। कमरे के तापमान और 1,132 ° C (2,070 ° F) के पिघलने के बिंदु के बीच, यूरेनियम धातु तीन क्रिस्टलीय रूपों में मौजूद है जिन्हें अल्फा (α), बीटा (β), और गामा (γ) चरणों के रूप में जाना जाता है। अल्फा से बीटा चरण में परिवर्तन 668 ° C (1,234 ° F) पर और बीटा से गामा चरण में 775 ° C (1,427 ° F) पर होता है। गामा यूरेनियम में एक शरीर-केंद्रित क्यूबिक (बीसीसी) क्रिस्टल संरचना है, जबकि बीटा यूरेनियम में टेट्रागोनल संरचना है। हालांकि, अल्फ़ा चरण में अत्यधिक विषमतापूर्ण ऑर्थोरोम्बिक संरचना में परमाणुओं की नालीदार चादरें होती हैं। यह अनिसोट्रोपिक, या विकृत, संरचना मिश्र धातु के परमाणुओं के लिए यूरेनियम परमाणुओं के विकल्प के लिए या क्रिस्टल जाली में यूरेनियम परमाणुओं के बीच रिक्त स्थान पर कब्जा करने के लिए मुश्किल बनाती है। केवल मोलिब्डेनम और नाइओबियम को यूरेनियम के साथ ठोस-घोल मिश्र बनाने के लिए देखा गया है।
इतिहास
जर्मन रसायनज्ञ मार्टिन हेनरिक क्लैप्रोथ को 1789 में पाइब्लब्लू के एक नमूने में तत्व यूरेनियम की खोज करने का श्रेय दिया जाता है। क्लैरोथ ने यूरेनस ग्रह के बाद नए तत्व का नाम दिया, जिसे 1781 में खोजा गया था। हालांकि, यह 1841 तक नहीं था, लेकिन फ्रांसीसी रसायनज्ञ यूजीन-मेलचियर पेलेगॉट ने दिखाया कि क्लैप्रोथ द्वारा प्राप्त काली धातु वास्तव में यौगिक यूरेनियम डाइऑक्साइड थी। पोटिगॉट ने पोटेशियम धातु के साथ यूरेनियम टेट्राक्लोराइड को कम करके वास्तविक यूरेनियम धातु तैयार की।
परमाणु विखंडन की खोज और मायावीकरण से पहले, यूरेनियम के कुछ व्यावहारिक उपयोग (और ये बहुत छोटे थे) मिट्टी के पात्र के रंग में और कुछ विशेष अनुप्रयोगों में उत्प्रेरक के रूप में थे। आज, परमाणु अनुप्रयोगों के लिए यूरेनियम अत्यधिक मूल्यवान है, दोनों सैन्य और वाणिज्यिक, और यहां तक कि निम्न-श्रेणी के अयस्कों में महान आर्थिक मूल्य हैं। यूरेनियम राज्य विश्वविद्यालय, एम्स में 1942 में अमेरिकी रसायनज्ञ एफएच स्पेडिंग और उनके सहयोगियों द्वारा विकसित एम्स प्रक्रिया के माध्यम से यूरेनियम धातु का नियमित रूप से उत्पादन किया जाता है। इस प्रक्रिया में मैग्नीशियम के साथ थर्मल कमी से यूरेनियम टेट्राफ्लोराइड से धातु प्राप्त की जाती है।
अयस्कों
पृथ्वी की पपड़ी में प्रति मिलियन यूरेनियम के लगभग दो भाग होते हैं, जो प्रकृति में व्यापक वितरण को दर्शाता है। समुद्र में 4.5 × 10 9 टन तत्व होने का अनुमान है । यूरेनियम 150 से अधिक विभिन्न खनिजों में महत्वपूर्ण घटक के रूप में और अन्य 50 खनिजों के एक मामूली घटक के रूप में होता है। प्राथमिक यूरेनियम खनिज, जो मैग्माटिक हाइड्रोथर्मल नसों में और पेगमाटाइट्स में पाए जाते हैं, में यूरेनैनेट और पिचब्लेंड (बाद में यूरेन्टी की एक किस्म) शामिल हैं। इन दोनों अयस्कों में यूरेनियम यूरेनियम डाइऑक्साइड के रूप में होता है, जो कि ऑक्सीकरण के कारण- सटीक रासायनिक संरचना में यूओ 2 से यूओ 2.67 तक भिन्न हो सकता है । आर्थिक महत्व के अन्य यूरेनियम अयस्कों, एक हाइड्रेटेड कैल्शियम यूरेनॉल फॉस्फेट हैं; tobernite, एक हाइड्रेटेड कॉपर uranyl फॉस्फेट; अनौपचारिक, एक काले हाइड्रेटेड यूरेनियम सिलिकेट; और कैनोनाइट, एक पीले हाइड्रेटेड पोटेशियम यूरेनिल वैनडेट।
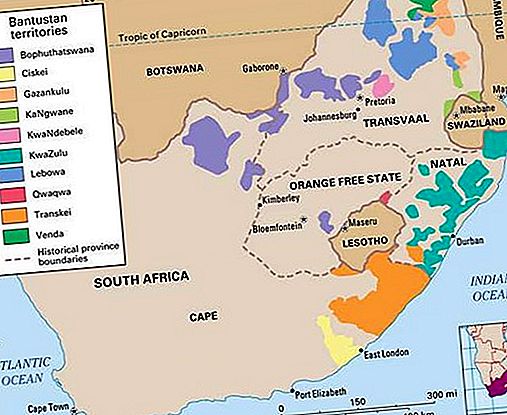
यह अनुमान है कि कनाडा, दक्षिण अफ्रीका, संयुक्त राज्य अमेरिका, ऑस्ट्रेलिया, नाइजर, नामीबिया, ब्राजील, अल्जीरिया और फ्रांस में 90 प्रतिशत से अधिक ज्ञात कम लागत वाले यूरेनियम भंडार हैं। इन भंडारों में से लगभग 50 से 60 प्रतिशत भण्डार, ओंटारियो में हूरों की झील के उत्तर में स्थित इलियट झील के विशाल चट्टान निर्माणों में हैं, और कैनवेट और दक्षिण अफ्रीका के विटवाटरसैंड गोल्डफील्ड्स में हैं। कोलोराडो पठार में बलुआ पत्थर के निर्माण और पश्चिमी संयुक्त राज्य के व्योमिंग बेसिन में भी यूरेनियम के महत्वपूर्ण भंडार हैं।
खनन और ध्यान केंद्रित
यूरेनियम के अयस्क जमाव में होते हैं जो कि निकट-सतह और बहुत गहरे (उदाहरण के लिए, 300 से 1,200 मीटर या 1,000 से 4,000 मीटर) होते हैं। गहरे अयस्कों में कभी-कभी 30 मीटर तक का भाग होता है। जैसा कि अन्य धातुओं के अयस्कों के साथ होता है, सतह यूरेनियम अयस्कों को बड़े पृथ्वी-गति वाले उपकरणों के साथ आसानी से खनन किया जाता है, जबकि पारंपरिक ऊर्ध्वाधर-शाफ्ट और बहाव विधियों द्वारा गहरी जमाओं का खनन किया जाता है।
यूरेनियम के अयस्कों में आमतौर पर केवल यूरेनियम-असर वाले खनिजों की एक छोटी मात्रा होती है, और ये प्रत्यक्ष पाइरोमेटालर्जिकल विधियों द्वारा गलाने के लिए उत्तरदायी नहीं हैं; इसके बजाय, यूरेनियम मूल्यों को निकालने और शुद्ध करने के लिए हाइड्रोमेटालर्जिकल प्रक्रियाओं का उपयोग किया जाना चाहिए। शारीरिक सांद्रता हाइड्रोमेटालार्जिकल प्रोसेसिंग सर्किट पर लोड को बहुत कम कर देगी, लेकिन आम तौर पर खनिज प्रसंस्करण में नियोजित पारंपरिक लाभकारी विधियों में से कोई भी नहीं है - उदाहरण के लिए, गुरुत्वाकर्षण, प्लवनशीलता, इलेक्ट्रोस्टैटिक्स, और यहां तक कि हाथ छांटना- आमतौर पर यूरेनियम अयस्कों पर लागू होते हैं। कुछ अपवादों के साथ, सांद्रता के तरीकों से यूरेनियम की टेलिंग में अत्यधिक हानि होती है।