यूरेनियम (यू), आवर्त सारणी के एक्टिनोइड श्रृंखला के रेडियोधर्मी रासायनिक तत्व, परमाणु संख्या 92। यह एक महत्वपूर्ण परमाणु ईंधन है।
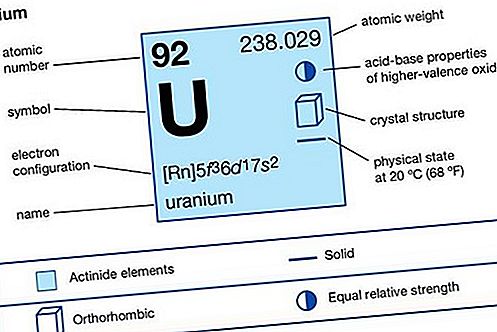

एक्टिनॉइड तत्व
।
यूरेनियम (सबसे परिचित) सहित समूह के सदस्य स्वाभाविक रूप से होते हैं, अधिकांश मानव निर्मित होते हैं। यूरेनियम और प्लूटोनियम दोनों का उपयोग किया गया है
।
यूरेनियम का गठन पृथ्वी की पपड़ी के प्रति मिलियन के दो भागों के बारे में है। कुछ महत्वपूर्ण यूरेनियम खनिज हैं पिचब्लेंड (अशुद्ध यू 3 ओ 8), यूरेनटीन (यूओ 2), कार्नोइट (एक पोटेशियम यूरेनियम वेनेडेट), ऑटुनाइट (एक कैल्शियम यूरेनियम फॉस्फेट), और टॉरनेनाइट (एक तांबे यूरेनियम फॉस्फेट)। ये और अन्य पुनर्प्राप्ति योग्य यूरेनियम अयस्कों, परमाणु ईंधन के स्रोतों के रूप में, जीवाश्म ईंधन के सभी ज्ञात पुनर्प्राप्ति योग्य जमाओं की तुलना में कई गुना अधिक ऊर्जा होते हैं। यूरेनियम का एक पाउंड कोयले की 1.4 मिलियन किलोग्राम (3 मिलियन पाउंड) जितनी ऊर्जा देता है।
यूरेनियम अयस्क जमा के बारे में अतिरिक्त जानकारी के लिए, साथ ही खनन, शोधन और पुनर्प्राप्ति तकनीकों के कवरेज में, यूरेनियम प्रसंस्करण देखें। यूरेनियम उत्पादन पर तुलनात्मक सांख्यिकीय आंकड़ों के लिए, तालिका देखें।
यूरेनियम
| देश | मेरा उत्पादन 2013 (मीट्रिक टन) | विश्व खदान उत्पादन का% |
|---|---|---|
| *आकलन। | ||
| स्रोत: विश्व परमाणु संघ, विश्व यूरेनियम खनन उत्पादन (2014)। | ||
| कजाखस्तान | 22,574 | 37.9 |
| कनाडा | 9332 | 15.6 |
| ऑस्ट्रेलिया | 6,350 | 10.6 |
| नाइजर * | 4528 | 7.6 |
| नामीबिया | 4315 | 7.2 |
| रूस | 3,135 | 5.3 |
| उज़्बेकिस्तान * | 2,400 | 4.0 |
| संयुक्त राज्य अमेरिका | 1,835 | 3.1 |
| चीन* | 1,450 | 2.4 |
| मलावी | 1,132 | 1.9 |
| यूक्रेन | 1,075 | 1.9 |
| दक्षिण अफ्रीका | 540 | 0.9 |
| भारत* | 400 | 0.7 |
| चेक गणतंत्र | 225 | 0.4 |
| ब्राज़िल | 198 | 0.3 |
| रोमानिया * | 80 | 0.1 |
| पाकिस्तान * | 41 | 0.1 |
| जर्मनी | 27 | 0.0 |
| दुनिया कुल | 59,637 | 100 |
यूरेनियम एक सघन, कठोर धात्विक तत्व है जो रंग में सफेद रंग का होता है। यह नमनीय, निंदनीय है, और उच्च पॉलिश लेने में सक्षम है। हवा में धातु धूमिल होती है और जब सूक्ष्म रूप से विभाजित लपटों में टूट जाती है। यह बिजली का अपेक्षाकृत खराब संवाहक है। हालांकि जर्मन रसायनज्ञ मार्टिन हेनरिक क्लैरोथ द्वारा खोजा गया (1789), जिसने हाल ही में खोजे गए ग्रह यूरेनस के नाम पर रखा था, धातु को पहले यूरेनियम टेट्राक्लोराइड (UCl 4) के साथ फ्रांसीसी रसायनज्ञ यूजीन-मेल्चीयर पेइजियोट द्वारा अलग किया गया था। पोटैशियम।
1869 में रूसी रसायनज्ञ दिमित्री मेंडेलीव द्वारा आवधिक प्रणाली के निर्माण ने यूरेनियम पर सबसे भारी रासायनिक तत्व के रूप में ध्यान केंद्रित किया, यह एक स्थिति है जो 1940 में पहले ट्रांस्यूरैनियम तत्व नेप्ट्यूनियम की खोज तक आयोजित की गई थी। 1896 में फ्रांसीसी भौतिक विज्ञानी हेनरी यूरेनियम में यूरेनियम की खोज की गई थी। रेडियोधर्मिता की घटना, पहली बार 1898 में फ्रांसीसी भौतिकविदों मैरी और पियरे क्यूरी द्वारा उपयोग की गई। यह संपत्ति बाद में कई अन्य तत्वों में मिली थी। अब यह ज्ञात है कि अपने सभी समस्थानिकों में यूरेनियम, रेडियोधर्मी, स्वाभाविक रूप से यूरेनियम -238 (99.27 प्रतिशत, 4,510,000,000-वर्ष का अर्ध-जीवन), यूरेनियम -235 (0.72 प्रतिशत, 7,000,000,000-वर्ष का अर्ध-जीवन) का मिश्रण होता है, और यूरेनियम -234 (0.006 प्रतिशत, 247,000-वर्ष आधा जीवन)। ये लंबे आधे जीवन कुछ यूरेनियम युक्त चट्टानों में सीसा, यूरेनियम के अंतिम क्षय उत्पाद की मात्रा को मापकर पृथ्वी की उम्र का निर्धारण करते हैं। यूरेनियम -238 रेडियोधर्मी यूरेनियम क्षय श्रृंखला में माता-पिता और यूरेनियम -234 बेटियों में से एक है; यूरेनियम -235 एक्टिनियम क्षय श्रृंखला का जनक है। एक्टिनॉइड तत्व भी देखें।
जर्मन रसायनज्ञ ओटो हैन और फ्रिट्ज स्ट्रैसमैन ने 1938 के अंत में यूरेनियम में परमाणु विखंडन की घटना की धीमी न्यूट्रॉन द्वारा बमबारी की खोज के बाद तत्व यूरेनियम गहन अध्ययन और व्यापक रुचि का विषय बन गया। इटली में जन्मे अमेरिकी भौतिक विज्ञानी एनरिको फर्मी ने सुझाव दिया (1939 के आरंभ में) कि न्यूट्रॉन विखंडन उत्पादों में से हो सकते हैं और इस प्रकार श्रृंखला प्रतिक्रिया के रूप में विखंडन जारी रख सकते हैं। हंगेरियन में जन्मे अमेरिकी भौतिक विज्ञानी लियो स्ज़ीलार्ड, अमेरिकी भौतिक विज्ञानी हरबर्ट एल एंडरसन, फ्रांसीसी रसायनज्ञ फ्रैडरिक जूलियट-क्यूरी और उनके सहकर्मियों ने इस भविष्यवाणी की पुष्टि की (1939); बाद में जांच से पता चला कि 2 के एक औसत 1 / 2 परमाणु प्रति न्यूट्रॉन विखंडन के दौरान जारी कर रहे हैं। उन खोजों ने पहली आत्मनिर्भर परमाणु श्रृंखला प्रतिक्रिया (2 दिसंबर, 1942) को जन्म दिया, पहला परमाणु बम परीक्षण (16 जुलाई, 1945), पहला परमाणु बम युद्ध में गिरा (6 अगस्त, 1945), पहला परमाणु संचालित पनडुब्बी (1955), और पहला पूर्ण पैमाने पर परमाणु ऊर्जा संचालित विद्युत जनरेटर (1957)।
विखंडन अपेक्षाकृत दुर्लभ आइसोटोप यूरेनियम -235 (केवल प्राकृतिक रूप से पाए जाने वाले फिसल सामग्री) में धीमी न्यूट्रॉन के साथ होता है, जिसे इसके विभिन्न उपयोगों के लिए भरपूर मात्रा में आइसोटोप यूरेनियम -238 से अलग किया जाना चाहिए। यूरेनियम -238, हालांकि, न्यूट्रॉन को अवशोषित करने और नकारात्मक बीटा क्षय से गुजरने के बाद, सिंथेटिक तत्व प्लूटोनियम में स्थानांतरित कर दिया जाता है, जो धीमे न्यूट्रॉन के साथ फिसल जाता है। इसलिए, प्राकृतिक यूरेनियम का उपयोग कनवर्टर और ब्रीडर रिएक्टरों में किया जा सकता है, जिसमें विखंडन दुर्लभ यूरेनियम -235 द्वारा होता है और प्लूटोनियम एक ही समय में यूरेनियम -238 के संचरण द्वारा निर्मित होता है। नॉनफिसाइल थोरियम आइसोटोप थोरियम -232 से परमाणु ईंधन के रूप में उपयोग के लिए फिशाइल यूरेनियम -233 को संश्लेषित किया जा सकता है, जो प्रकृति में प्रचुर मात्रा में है। यूरेनियम प्राथमिक सामग्री के रूप में भी महत्वपूर्ण है जिसमें से सिंथेटिक ट्रांसूरानियम तत्वों को संवातन प्रतिक्रियाओं द्वारा तैयार किया गया है।
यूरेनियम, जो दृढ़ता से इलेक्ट्रोपोसिटिव है, पानी से प्रतिक्रिया करता है; यह एसिड में घुलता है लेकिन क्षार में नहीं। महत्वपूर्ण ऑक्सीकरण अवस्थाएं +4 हैं (जैसा कि ऑक्साइड यूओ 2 में, टेट्राहलाइड्स जैसे यूसीएल 4, और हरे रंग का जलीय आयन यू 4 +) और +6 (जैसा कि ऑक्साइड यूओ 3 में, हेक्साक्लोराइड यूएफ 6, और पीले यूरैनल में होता है) आयन यूओ 2 2+)। एक जलीय घोल में यूरेनियम आयन के रूप में सबसे अधिक स्थिर होता है, जिसमें एक रैखिक संरचना होती है [O = U = O] 2+ । यूरेनियम एक +3 और +5 स्थिति भी प्रदर्शित करता है, लेकिन संबंधित आयन अस्थिर होते हैं। लाल यू 3+ आयन पानी में भी धीरे-धीरे ऑक्सीकरण करता है जिसमें कोई भंग ऑक्सीजन नहीं होता है। यूओ 2 + आयन का रंग अज्ञात है, क्योंकि यह विघटित हो जाता है (यूओ 2 + एक साथ यू 4 + तक कम हो जाता है और बहुत पतला समाधानों में भी यूओ 2 2+ के लिए ऑक्सीकरण होता है)।
यूरेनियम यौगिकों को सिरेमिक के लिए रंग एजेंटों के रूप में उपयोग किया गया है। यूरेनियम हेक्साफ्लोराइड (UF 6) 25 डिग्री सेल्सियस (77 ° F) पर असामान्य रूप से उच्च वाष्प दबाव (115 torr = 0.15 atm = 15,300 Pa) के साथ एक ठोस है। यूएफ 6 रासायनिक रूप से बहुत प्रतिक्रियाशील है, लेकिन, वाष्प अवस्था में इसकी संक्षारक प्रकृति के बावजूद, यूएफ 6 को यूरेनियम -238 से यूरेनियम -235 को अलग करने के लिए गैस-प्रसार और गैस-अपकेंद्रित्र विधियों में व्यापक रूप से उपयोग किया गया है।
ऑर्गोनोमेटेलिक यौगिक यौगिकों का एक दिलचस्प और महत्वपूर्ण समूह है जिसमें धातु-कार्बन बांड होते हैं जो एक धातु को कार्बनिक समूहों से जोड़ते हैं। यूरेनोसिन एक ऑर्गेनोमीन यौगिक यू (सी 8 एच 8) 2 है, जिसमें एक यूरेनियम परमाणु दो कार्बनिक रिंग परतों के बीच cyclooctatetraene C 8 H 8 से संबंधित है । 1968 में इसकी खोज ने ऑर्गेनोमेट्रिक रसायन विज्ञान का एक नया क्षेत्र खोल दिया।
तत्व गुण
| परमाणु क्रमांक | 92 |
|---|---|
| परमाण्विक भार | 238.03 |
| गलनांक | 1,132.3 ° C (2,070.1 ° F) |
| क्वथनांक | 3,818 ° C (6,904 ° F) |
| विशिष्ट गुरुत्व | 19.05 |
| ऑक्सीकरण स्थिति | +3, +4, +5, +6 |
| गैसीय परमाणु अवस्था का इलेक्ट्रॉन विन्यास | [आरएन] ५ एफ ३ ६ डी १ n एस २ |






![बेनेल डे द्वारा बेले डे पत्रिका फिल्म [1967] बेनेल डे द्वारा बेले डे पत्रिका फिल्म [1967]](https://images.thetopknowledge.com/img/entertainment-pop-culture/3/belle-de-jour-film-buuel-1967.jpg)