स्कैंडियम (एससी), रासायनिक तत्व, आवर्त सारणी के समूह 3 की एक दुर्लभ-पृथ्वी धातु।
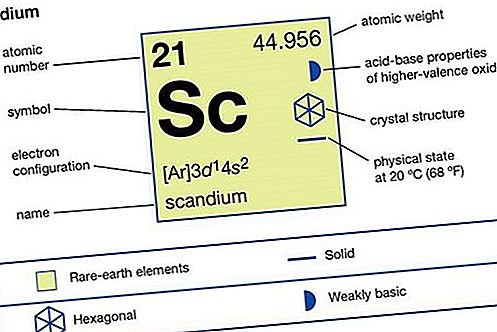
स्कैंडियम एक चांदी सफेद, मध्यम नरम धातु है। यह हवा में काफी स्थिर है, लेकिन सतह पर स्क 2 ओ 3 ऑक्साइड के गठन के कारण धीरे-धीरे इसका रंग सिलवरी सफेद से पीले रंग में बदल जाएगा । धातु धीरे-धीरे पतला एसिड में घुल जाती है - हाइड्रोफ्लोरिक एसिड (एचएफ) को छोड़कर, जिसमें एक सुरक्षात्मक ट्राइफ्लोराइड परत आगे की प्रतिक्रिया को रोकती है। स्कैंडियम 0 K (°273 ° C, या is460 ° F) से इसके गलनांक (1,541 ° C, या 2,806 ° F) तक अर्धचालक है। यह 186 किलोग्राम से अधिक दबाव में 3273.1 ° C (.6459.6 ° F) पर अतिचालक हो जाता है।
1871 में रूसी रसायनशास्त्री दिमित्री इवानोविच मेंडेलेयेव ने इस तत्व के अस्तित्व की भविष्यवाणी की, इसे अस्थायी रूप से एक्कोबोरन कहा, 1879 में स्वीडिश रसायनज्ञ लार्स फ्रेड्रिक निल्सन ने दुर्लभ पृथ्वी खनिजों के गैडोलीन और इक्सेनाईट में ऑक्साइड, स्कैंडिया की खोज की, और स्वीडिश रसायनज्ञ प्रति टोडोर क्लीव ने 1879 में। काल्पनिक स्कंध के रूप में स्कैंडियम की पहचान की। स्कैंडियम छोटे अनुपात में पाया जाता है, आम तौर पर 0.2 प्रतिशत से कम, कई भारी लैंथेनाइड अयस्कों में और कई टिन, यूरेनियम और टंगस्टन अयस्कों में। Thortveitite (एक स्कैंडियम सिलिकेट) एकमात्र खनिज है जिसमें लगभग 34 प्रतिशत स्कैंडियम की बड़ी मात्रा होती है, लेकिन दुर्भाग्य से यह खनिज काफी दुर्लभ है और स्कैंडियम का एक महत्वपूर्ण स्रोत नहीं है। स्कैंडियम की लौकिक बहुतायत अपेक्षाकृत अधिक है। यद्यपि यह पृथ्वी पर केवल 50 वें सबसे प्रचुर तत्व के बारे में है (इसकी प्रचुरता बेरिलियम के समान है), यह सूर्य में 23 वें सबसे प्रचुर तत्व के बारे में है।
प्रकृति में, स्कैंडियम एक स्थिर आइसोटोप, स्कैंडियम -45 के रूप में मौजूद है। 25 से (परमाणु आइसोमर्स को छोड़कर) 36 से 61 तक के द्रव्यमान वाले रेडियोधर्मी आइसोटोप, सबसे अधिक स्थिर स्कैंडियम -46 (83.79 दिनों का अर्ध-जीवन) है, और सबसे कम स्थिर स्कैंडियम -39 (300 नैनोसेकेंड से कम का आधा जीवन) है)।
स्कैंडियम को अघुलनशील पोटेशियम स्कैंडियम सल्फेट की वर्षा या डायथाइल ईथर द्वारा स्कैंडियम थियोसाइनेट के निष्कर्षण द्वारा अन्य दुर्लभ पृथ्वी से अलग किया जाता है। धातु को पहली बार 1938 में पोटेशियम, लिथियम और स्कैंडियम क्लोराइड के इलेक्ट्रोलिसिस द्वारा एक यूक्टेक्टिक मिश्रण में तैयार किया गया था (यानी, उन घटकों के साथ सबसे कम पिघलने बिंदु संभव है)। स्कैंडियम अब खनिज डेविडे से यूरेनियम निष्कर्षण के उप-उत्पाद के रूप में उत्पादित किया जाता है, जिसमें लगभग 0.02 प्रतिशत स्कैंडियम ऑक्साइड होता है। स्कैंडियम दो एलोट्रोपिक (संरचनात्मक) रूपों में मौजूद है। Α-चरण कमरे के तापमान पर = 3.3088 c और c = 5.2680 is के साथ करीब-पैक हेक्सागोनल है। The-चरण शरीर-केंद्रित घन है जिसका अनुमानित = 3.73 Å 1,337 ° C (2,439 ° F) है।
इस असामान्य संक्रमण धातु के केवल कुछ उपयोग विकसित किए गए हैं, ज्यादातर स्कैंडियम की सीमित उपलब्धता और उच्च लागत के कारण। इसकी कम घनत्व और उच्च गलनांक सैन्य और उच्च प्रदर्शन अनुप्रयोगों के लिए हल्के धातुओं के लिए एक मिश्र धातु एजेंट के रूप में अनुप्रयोगों का सुझाव देते हैं। स्कैंडियम के प्रमुख उपयोग खेल के सामान के लिए एल्यूमीनियम आधारित मिश्र धातु और उच्च तीव्रता वाले धातु हलाइड लैंप में मिश्र धातु के रूप में होते हैं। जब एल्यूमीनियम और एल्यूमीनियम-आधारित मिश्र धातुओं के साथ मिश्र धातु, स्कैंडियम उच्च तापमान वाले अनाज के विकास को सीमित करता है।
स्कैंडियम की रसायन ऑक्सीकरण राज्य +3 के अन्य दुर्लभ-पृथ्वी तत्वों की तुलना में एल्यूमीनियम या टाइटेनियम की तुलना में अधिक निकट है। हालांकि, इसके कुछ व्यवहार दुर्लभ पृथ्वी के प्रायश्चितिक हैं, क्योंकि इसके छोटे आयनिक त्रिज्या (समन्वय संख्या 12 के लिए 1.66 however) की तुलना में दुर्लभ-पृथ्वी औसत (समन्वय संख्या 12 के लिए 1.82 however) की तुलना में है। इस कारण से, Sc 3+ आयन एक अपेक्षाकृत मजबूत एसिड है और इसमें जटिल आयन बनाने की बहुत अधिक प्रवृत्ति है।
तत्व गुण
| परमाणु क्रमांक | 21 |
|---|---|
| परमाण्विक भार | ४४.९५,५९१ |
| गलनांक | 1,541 ° C (2,806 ° F) |
| क्वथनांक | 2,836 ° C (5,137 ° F) |
| विशिष्ट गुरुत्व | 2.989 (24 ° C, या 75 ° F) |
| ऑक्सीकरण अवस्था | +3 |
| ऋणावेशित सूक्ष्म अणु का विन्यास | [अर] 3 डी 1 4 जी 2 |








![द बिग स्लीप फिल्म हॉक्स द्वारा [1946] द बिग स्लीप फिल्म हॉक्स द्वारा [1946]](https://images.thetopknowledge.com/img/entertainment-pop-culture/6/big-sleep-film-hawks-1946.jpg)