ऑक्सीसायड, किसी भी ऑक्सीजन युक्त एसिड। अधिकांश सहसंयोजक अधातु ऑक्साइड अम्लीय ऑक्साइड बनाने के लिए पानी के साथ प्रतिक्रिया करते हैं; यही है, वे समाधान में हाइड्रोनियम आयन (एच 3 ओ +) प्राप्त करने वाले ऑक्साक्साइड बनाने के लिए पानी के साथ प्रतिक्रिया करते हैं। कुछ अपवाद हैं, जैसे कार्बन मोनोऑक्साइड, CO, नाइट्रस ऑक्साइड, N 2 O और नाइट्रिक ऑक्साइड, NO।
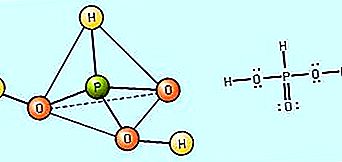
एक ऑक्सीसिड की ताकत को उस हद तक परिभाषित किया जाता है जिससे यह पानी में भंग हो जाता है (यानी, एच + आयनों के निर्माण की क्षमता)। सामान्य तौर पर, ऑक्सीकॉइड की सापेक्ष शक्ति का अनुमान केंद्रीय गैर-परमाणु परमाणु की इलेक्ट्रोनगेटिविटी और ऑक्सीकरण संख्या के आधार पर लगाया जा सकता है। केंद्रीय परमाणु के इलेक्ट्रोनगेटिविटी बढ़ने पर एसिड की ताकत बढ़ जाती है। उदाहरण के लिए, क्योंकि क्लोरीन (Cl) की इलेक्ट्रोनगेटिविटी सल्फर (S) की तुलना में अधिक होती है, जो कि फॉस्फोरस (P) की तुलना में अधिक होती है, यह अनुमान लगाया जा सकता है कि पर्क्लोरिक एसिड, HClO 4, की तुलना में अधिक मजबूत एसिड है। सल्फ्यूरिक एसिड, एच 2 एसओ 4, जो फॉस्फोरिक एसिड, एच 3 पीओ 4 से अधिक मजबूत एसिड होना चाहिए। किसी दिए गए अधातु केंद्रीय परमाणु के लिए, एसिड की शक्ति बढ़ जाती है क्योंकि केंद्रीय परमाणु की ऑक्सीकरण संख्या बढ़ जाती है। उदाहरण के लिए, नाइट्रिक एसिड, HNO 3, जिसमें नाइट्रोजन (N) परमाणु का ऑक्सीकरण संख्या +5 है, नाइट्रस एसिड, HNO 2 की तुलना में अधिक मजबूत एसिड है, जहां नाइट्रोजन ऑक्सीकरण राज्य +3 है। उसी प्रकार, सल्फर एसिड, एच 2 एसओ 4, सल्फर के साथ इसकी +6 ऑक्सीकरण अवस्था में, सल्फर एसिड, एच 2 एसओ 3 की तुलना में अधिक मजबूत एसिड है, जहां सल्फर का +4 ऑक्सीकरण संख्या मौजूद है।
जब एक आधार के साथ अम्ल प्रतिक्रिया करता है तो ऑक्सीकाइड का नमक एक यौगिक बनता है: अम्ल + क्षार → नमक + पानी। इस तरह की प्रतिक्रिया को न्यूट्रलाइजेशन कहा जाता है, क्योंकि समाधान को तटस्थ बनाया जाता है।