नोबल गैस, आवर्त सारणी के समूह 18 (VIIIa) बनाने वाले सात रासायनिक तत्वों में से कोई भी। तत्व हीलियम (He), नियोन (Ne), आर्गन (Ar), क्रिप्टन (Kr), क्सीनन (Xe), रेडॉन (Rn) और ओगेनेसन (Og) हैं। नेक गैसें रंगहीन, गंधहीन, बेस्वाद, बिना गंध वाली गैसें होती हैं। उन्हें परंपरागत रूप से आवर्त सारणी में समूह 0 का लेबल दिया गया है क्योंकि उनकी खोज के बाद दशकों तक यह माना जाता था कि वे अन्य परमाणुओं से बंध नहीं सकते थे; यह है, कि उनके परमाणु रासायनिक यौगिकों को बनाने के लिए अन्य तत्वों के साथ संयोजन नहीं कर सकते हैं। उनकी इलेक्ट्रॉनिक संरचनाएं और यह पता लगाना कि उनमें से कुछ वास्तव में यौगिक बनाते हैं, ने अधिक उपयुक्त पदनाम समूह 18 का नेतृत्व किया है।
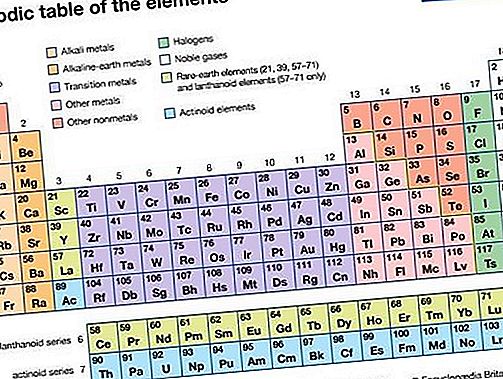
जब समूह के सदस्यों की खोज और पहचान की गई, तो उन्हें अत्यधिक दुर्लभ माना जाता था, साथ ही रासायनिक रूप से निष्क्रिय भी, और इसलिए उन्हें दुर्लभ या अक्रिय गैस कहा जाता था। हालांकि, अब यह ज्ञात है कि इनमें से कई तत्व पृथ्वी पर और बाकी ब्रह्मांड में काफी प्रचुर मात्रा में हैं, इसलिए यह पदनाम दुर्लभ भ्रामक है। इसी प्रकार, शब्द का उपयोग अक्रिय में यह दोष है कि यह रासायनिक निष्क्रियता को दर्शाता है, यह सुझाव देता है कि समूह 18 के यौगिकों का गठन नहीं किया जा सकता है। रसायन विज्ञान और कीमिया में, महान शब्द ने धातु की अनिच्छा को इंगित किया है, जैसे कि सोना और प्लैटिनम, रासायनिक प्रतिक्रिया से गुजरना; यह यहाँ पर गैसों के समूह के लिए समान अर्थ में लागू होता है।
जैसे-जैसे उनकी परमाणु संख्या बढ़ती जाती है महान गैसों की प्रचुरता कम होती जाती है। हाइड्रोजन को छोड़कर हीलियम ब्रह्मांड में सबसे भरपूर तत्व है। पृथ्वी के वायुमंडल में सभी महान गैस मौजूद हैं और हीलियम और रेडॉन को छोड़कर, उनका प्रमुख वाणिज्यिक स्रोत हवा है, जहां से उन्हें द्रवीकरण और आंशिक आसवन द्वारा प्राप्त किया जाता है। अधिकांश हीलियम का उत्पादन कुछ प्राकृतिक गैस कुओं से व्यावसायिक रूप से किया जाता है। रेडॉन आमतौर पर रेडियम यौगिकों के रेडियोधर्मी अपघटन के उत्पाद के रूप में पृथक होता है। रेडियम परमाणुओं के नाभिक अनायास ऊर्जा और कणों, हीलियम नाभिक (अल्फा कणों) और रेडॉन परमाणुओं का उत्सर्जन करके क्षय करते हैं। महान गैसों के कुछ गुण तालिका में सूचीबद्ध हैं।
महान गैसों के कुछ गुण
| हीलियम | नीयन | आर्गन | क्रीप्टोण | क्सीनन | राडोण | युनुनोक्टियम | |
|---|---|---|---|---|---|---|---|
| * 25.05 वायुमंडल पर। | |||||||
| ** एचसीपी = हेक्सागोनल क्लोज-पैक, एफसी = फेस-सेंटेड क्यूबिक (क्यूबिक क्लोज-पैक)। | |||||||
| *** स्टैब्लेट्स आइसोटोप। | |||||||
| परमाणु क्रमांक | 2 | 10 | 18 | 36 | 54 | 86 | 118 |
| परमाण्विक भार | 4.003 | 20.18 | 39.948 | 83.8 | 131.293 | 222 | 294 *** |
| गलनांक (° C) | -272.2 * | -248.59 | -189.3 | -157.36 | -111.7 | -71 | - |
| क्वथनांक (° C) | -268.93 | -246.08 | -185.8 | -153.22 | -108 | -61.7 | - |
| 0 डिग्री सेल्सियस पर घनत्व, 1 वायुमंडल (प्रति लीटर ग्राम) | .१७,८४७ | 0.899 | 1.784 | 3.75 | 5.881 | 9.73 | - |
| 20 डिग्री सेल्सियस पर पानी में घुलनशीलता (1,000 ग्राम पानी में घन सेंटीमीटर गैस) | 8.61 | 10.5 | 33.6 | 59.4 | 108.1 | 230 | - |
| समस्थानिक बहुतायत (स्थलीय, प्रतिशत) | 3 (0.000137), 4 (99.999863) | 20 (90.48), 21 (0.27), 22 (9.25) | 36 (0.3365), 40 (99.6003) | 78 (0.35), 80 (2.28), 82 (11.58), 83 (11.49), 84 (57), 86 (17.3) | 124 (0.09), 126 (0.09), 128 (1.92), 129 (26.44), 130 (4.08), 131 (21.18), 132 (26.89), 134 (10.44), 136 (8.87) | - | - |
| रेडियोधर्मी समस्थानिक (जन संख्या) | 5-10 | 16-19, 23-34 | 30-35, 37, 39, 41-53 | 69-77, 79, 81, 85, 87-100 | 110–125, 127, 133, 135–147 | 195-228 | 294 |
| गैसीय डिस्चार्ज ट्यूब द्वारा उत्सर्जित प्रकाश का रंग | पीला | लाल | लाल या नीला | पीला हारा | नीला से हरा | - | - |
| संलयन की ऊष्मा (प्रति किलो किलोजूल) | 0.02 | 0.34 | 1.18 | 1.64 | 2.3 | 3 | - |
| वाष्पीकरण की गर्मी (कैलोरी प्रति तिल) | 0.083 | 1.75 | 6.5 | 9.02 | 12.64 | 17 | - |
| विशिष्ट ऊष्मा (जूल प्रति ग्राम केल्विन) | 5.1931 | 1.03 | .५२,०३३ | .२४,८०५ | .१५,८३२ | .०९,३६५ | - |
| महत्वपूर्ण तापमान (K) | 5.19 | 44.4 | 150.87 | 209.41 | 289.77 | 377 | - |
| गंभीर दबाव (वायुमंडल) | 2.24 | 27.2 | 48.34 | 54.3 | 57.65 | 62 | - |
| महत्वपूर्ण घनत्व (ग्राम प्रति घन सेंटीमीटर) | 0.0696 | 0.4819 | 0.5356 | 0.9092 | 1.103 | - | - |
| तापीय चालकता (वाट प्रति मीटर केल्विन) | 0.1513 | 0.0491 | 0.0177 | 0.0094 | 0.0057 | 0.0036 | - |
| चुंबकीय संवेदनशीलता (प्रति तिल प्रति किलोग्राम) | -.००,००,०१९ | -.००,००,०७२ | -.००,००,१९४ | -.०,००,०२८ | -.०,००,०४३ | - | - |
| क्रिस्टल की संरचना** | HCP | एफसीसी | एफसीसी | एफसीसी | एफसीसी | एफसीसी | - |
| त्रिज्या: परमाणु (एंगस्ट्रॉम) | 0.31 | 0.38 | 0.71 | 0.88 | 1.08 | 1.2 | - |
| त्रिज्या: सहसंयोजक (क्रिस्टल) अनुमानित (एंग्स्ट्रॉम) | 0.32 | 0.69 | 0.97 | 1.1 | 1.3 | 1.45 | - |
| स्थैतिक ध्रुवीकरण (घन एंगस्ट्रॉम) | 0.204 | 0.392 | 1.63 | 2.465 | 4.01 | - | - |
| आयनीकरण क्षमता (पहले, इलेक्ट्रॉन वोल्ट) | 24.587 | 21.565 | 15.759 | 13.999 | 12.129 | 10.747 | - |
| वैद्युतीयऋणात्मकता (पॉलिंग) | 4.5 | 4.0 | 2.9 | 2.6 | 2.25 | 2.0 | - |