नाइट्रिक एसिड, (HNO 3), रंगहीन, धूआं और अत्यधिक संक्षारक तरल (हिमांक −42 ° C [C44 ° F], क्वथनांक 83 ° C [181 ° F]) जो एक सामान्य अभिकर्मक और एक महत्वपूर्ण अभिकर्मक है उर्वरकों और विस्फोटकों के निर्माण के लिए औद्योगिक रसायन। यह विषाक्त है और गंभीर जलन पैदा कर सकता है।
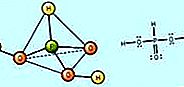
ऑक्सीसायड: नाइट्रिक एसिड और नाइट्रेट लवण
नाइट्रिक एसिड, एचएनओ 3, 8 वीं शताब्दी के रसायनविदों को "एक्वा फोर्टिस" (मजबूत पानी) के रूप में जाना जाता था। यह बनता है
।
नाइट्रिक एसिड की तैयारी और उपयोग प्रारंभिक रसायनज्ञों को पता था। कई वर्षों तक इस्तेमाल की जाने वाली एक सामान्य प्रयोगशाला प्रक्रिया, जो एक जर्मन रसायनज्ञ, जोहान रुडोल्फ ग्लुबेर (1648) को दी गई थी, जिसमें केंद्रित सल्फ्यूरिक एसिड के साथ पोटेशियम नाइट्रेट को गर्म करना शामिल था। 1776 में एंटोनी-लॉरेंट लावोइसियर ने दिखाया कि इसमें ऑक्सीजन था, और 1816 में जोसेफ-लुई गे-लुसाक और क्लाउड-लुइस बर्थोलेट ने अपनी रासायनिक संरचना स्थापित की।
नाइट्रिक एसिड के निर्माण की मुख्य विधि अमोनिया का उत्प्रेरक ऑक्सीकरण है। 1901 में जर्मन रसायनज्ञ विल्हेम ओस्टवाल्ड द्वारा विकसित विधि में, प्लैटिनम धुंध उत्प्रेरक की उपस्थिति में हवा या ऑक्सीजन द्वारा अमोनिया गैस को नाइट्रिक ऑक्साइड और नाइट्रोजन डाइऑक्साइड को क्रमिक रूप से ऑक्सीकरण किया जाता है। नाइट्रोजन डाइऑक्साइड को नाइट्रिक एसिड बनाने के लिए पानी में अवशोषित किया जाता है। परिणामी एसिड-इन-वॉटर सॉल्यूशन (वजन एसिड द्वारा लगभग 50-70 प्रतिशत) सल्फ्यूरिक एसिड के साथ आसवन द्वारा निर्जलित किया जा सकता है।
नाइट्रिक एसिड पानी, नाइट्रोजन डाइऑक्साइड और ऑक्सीजन में बदल जाता है, जिससे भूरे पीले रंग का घोल बनता है। यह एक मजबूत एसिड है, जलीय घोल में हाइड्रोनियम (H 3 O +) और नाइट्रेट (NO 3 -) आयनों में पूरी तरह से आयनित होता है, और एक शक्तिशाली ऑक्सीकरण एजेंट (ऑक्सीकरण-कमी प्रतिक्रियाओं में इलेक्ट्रॉन स्वीकर्ता के रूप में कार्य करता है)। नाइट्रिक एसिड की कई महत्वपूर्ण प्रतिक्रियाओं में से हैं: अमोनियम के साथ तटस्थकरण, अमोनियम नाइट्रेट बनाने के लिए, उर्वरकों का एक प्रमुख घटक; ग्लिसरॉल और टोल्यूनि का नाइट्रेशन, क्रमशः विस्फोटक नाइट्रोग्लिसरीन और ट्रिनिट्रोटोलुइन (टीएनटी) का निर्माण; नाइट्रोसेल्युलोज की तैयारी; और संबंधित ऑक्साइड या नाइट्रेट के लिए धातुओं का ऑक्सीकरण।