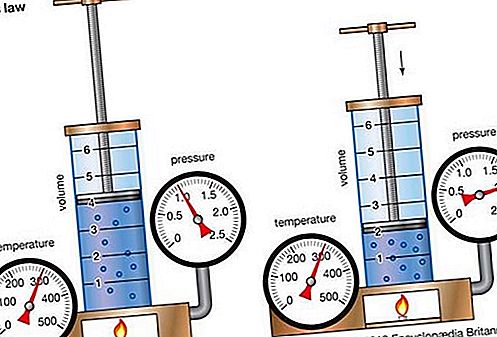
बॉयल के नियम, जिसे मारियट का नियम भी कहा जाता है, निरंतर तापमान पर गैस के संपीड़न और विस्तार से संबंधित एक संबंध है। भौतिकवादी रॉबर्ट बॉयल द्वारा 1662 में तैयार किए गए इस आनुभविक संबंध में कहा गया है कि गैस की दी गई मात्रा का दबाव (p) निरंतर तापमान पर इसकी मात्रा (v) के साथ भिन्न होता है; अर्थात, समीकरण रूप में, pv = k, a Contin। इस रिश्ते की खोज फ्रांसीसी भौतिक विज्ञानी एडमे मारियोटे (1676) ने भी की थी।
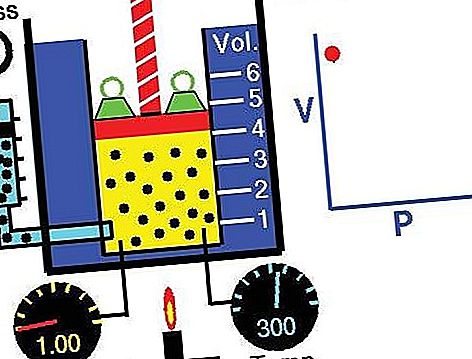
कानून को एक आदर्श (आदर्श) गैस (संपूर्ण गैस देखें) गैसों के गतिज सिद्धांत से प्राप्त किया जा सकता है। वास्तविक गैसें पर्याप्त रूप से कम दबाव पर बॉयल के नियम का पालन करती हैं, हालांकि उच्च दबाव पर उत्पाद pv आमतौर पर थोड़ा कम हो जाता है, जहां गैस आदर्श व्यवहार से प्रस्थान करना शुरू कर देता है।









![एंटीथम अमेरिकन सिविल वॉर की लड़ाई [1862] एंटीथम अमेरिकन सिविल वॉर की लड़ाई [1862]](https://images.thetopknowledge.com/img/world-history/0/battle-antietam-american-civil-war-1862.jpg)


![फोर्ड द्वारा द मैन हू शॉट लिबर्टी वैलेंस फिल्म [1962] फोर्ड द्वारा द मैन हू शॉट लिबर्टी वैलेंस फिल्म [1962]](https://images.thetopknowledge.com/img/entertainment-pop-culture/5/man-who-shot-liberty-valance-film-ford-1962.jpg)